- 印刷用
- 2016年3月28日
エーザイ株式会社(本社:東京都、代表執行役CEO:内藤晴夫)は、本日、自社創製の新規抗てんかん剤「フィコンパ®」(一般名:ペランパネル水和物、海外製品名「Fycompa®」)について、日本において、「他の抗てんかん薬で十分な効果が認められないてんかん患者の部分発作(二次性全般化発作を含む)および強直間代発作に対する抗てんかん薬との併用療法」の効能・効果で、承認を取得したことをお知らせします。
本承認は、日本とアジアにおける12歳以上の難治性部分てんかん患者様の部分発作に対する併用療法として実施した臨床第Ⅲ相試験(335試験)結果1、およびグローバルでの12歳以上の難治性全般てんかん患者様の強直間代発作に対する併用療法として実施した臨床第Ⅲ相試験(332試験)結果2に基づくものです。
335試験の主要評価項目である発作頻度変化率において、「フィコンパ」8mg群および12mg群は、プラセボ群と比較して統計学的に有意な減少を示しました。また、332試験の主要評価項目である強直間代発作頻度変化率においても、「フィコンパ」群はプラセボ群に比較して統計学的に有意な減少を示し、さらに「フィコンパ」群では30.9%の患者様において、治療維持期13週間にわたり強直間代発作がない状態(無発作状態:seizure free)が維持されました(プラセボ群では12.3%)。なお、335試験及び332試験において認められた一般的な有害事象(頻度10%以上かつプラセボ群より高頻度)は、浮動性めまい、疲労、頭痛、傾眠、易刺激性でした。
「フィコンパ」は、当社の筑波研究所で創製されたファースト・イン・クラスの抗てんかん剤であり、1日1回投与の錠剤です。本剤は、グルタミン酸によるシナプス後AMPA受容体の活性化を高選択的かつ非競合的に阻害し、神経の過興奮を抑制します。12歳以上のてんかん患者様の部分発作(二次性全般化発作を含む)に対する併用療法として欧米など45カ国以上で承認を取得しており、12歳以上の強直間代発作に対する併用療法についても欧米など35カ国以上で適応拡大の承認を取得しています。
日本におけるてんかん患者様数は約100万人と報告されています。てんかんは、患者様の約30%が既存の抗てんかん剤では発作を十分にコントロールできておらず3、アンメット・メディカル・ニーズの高い疾患です。また、強直間代発作は、突然の転倒による重篤なけがの恐れがあるほか、その発作頻度は「てんかん患者様の予期せぬ突然死(SUDEP: Sudden Unexpected Death in Epilepsy)」の最も重要な危険因子とされ4、てんかんの中でも極めて重篤な発作型の一つです。
当社は、ニューロロジー領域を重点疾患領域と位置づけており、日本においても抗てんかん薬「イノベロン®」や「ホストイン®」などに加えて、「フィコンパ」を新たな治療選択肢としてお届けすることにより、てんかん患者様とそのご家族の多様なニーズの充足とベネフィット向上により一層貢献してまいります。
以上
<参考資料>
1. 製品概要
- 1)
製品名
フィコンパ®錠2mg、フィコンパ®錠4mg
- 2)
一般名
ペランパネル水和物
- 3)
効能・効果
他の抗てんかん薬で十分な効果が認められないてんかん患者の下記発作に対する抗てんかん薬との併用療法
部分発作(二次性全般化発作を含む)
強直間代発作
- 4)用法・用量
通常、成人及び12歳以上の小児にはペランパネルとして1日1回2mgの就寝前経口投与より開始し、その後1週間以上の間隔をあけて2mgずつ漸増する。本剤の代謝を促進する抗てんかん薬を併用しない場合の維持用量は1日1回8mg、併用する場合の維持用量は1日1回8~12mgとする。なお、症状により1週間以上の間隔をあけて2mgずつ適宜増減するが、1日最高12mgまでとする。
2. 「フィコンパ」(一般名:ペランパネル水和物、海外製品名「Fycompa」)について
「フィコンパ」は、当社が創製したファースト・イン・クラスの抗てんかん剤です。てんかん発作は、神経伝達物質であるグルタミン酸により誘発されることが報告されており、本剤は、グルタミン酸によるシナプス後AMPA受容体の活性化を阻害し、神経の過興奮を抑制する高選択、非競合AMPA受容体拮抗剤です。本剤は1日1回経口投与する錠剤です。
本剤は、12歳以上のてんかん患者様の部分発作(二次性全般化発作を含む)に対する併用療法を適応として、欧米など45カ国以上で承認を取得しています。また、全般てんかん患者様の強直間代発作に対する併用療法について、欧米など35カ国以上で承認を取得しています。なお、米国では「12歳以上の全般てんかん患者様の強直間代発作に対する併用療法」の適応で、欧州では「12歳以上の特発性全般てんかん患者様の強直間代発作に対する併用療法」の適応で承認を取得しています。
日本では、2015年7月に新薬承認申請を行い、このたび、「他の抗てんかん薬で十分な効果が認められないてんかん患者の部分発作(二次性全般化発作を含む)および強直間代発作に対する抗てんかん薬との併用療法」の適応で承認を取得しました。
さらに、欧米にて懸濁液の剤型追加の承認申請を2015年6月に行いました。加えて、部分てんかんの小児患者様を対象に欧米で臨床第Ⅱ相試験を実施しています。
3. 335試験の概要1
※左右にスクロールできます
| 試験名称 | : | 部分発作を有する難治性てんかん患者様を対象とした他剤併用時における「フィコンパ」の有効性及び安全性を評価する多施設共同無作為化二重盲検プラセボ対照並行群間比較試験 |
|---|---|---|
| 対象 | : | 1∼3種類の抗てんかん剤治療を受けている部分発作を有する12歳以上の患者様710名 |
| 投与法 | : | 「フィコンパ」4mg/日、8mg/日、12mg/日、またはプラセボを1日1回就寝前に経口投与 |
| 治療期間 | : | 観察期 6週間 治療期(治療漸増期6週間及び治療維持期13週間) 19週間 継続投与期 10週間以上 |
| 実施地域 | : | 日本、中国、韓国、オーストラリア、タイ、マレーシア、台湾 |
| 主要評価項目 | : | 発作頻度変化率: 28日間あたりの発作頻度の観察期からの変化率 |
| 結果 | : | 発作頻度変化率は、「フィコンパ」4mg群、8mg群、12mg群およびプラセボ群で、それぞれ-17.3%、-29.0%、-38.0%および-10.8%であり、「フィコンパ」8mg群と12mg群においてプラセボ群と比較して統計学的に有意な減少を示しました(p=0.0003、p<0.0001)。 |
| 主な有害事象 | : | 「フィコンパ」群で10%より発生頻度が高く、かつプラセボ群より発生頻度が高い一般的な有害事象は、浮動性めまい(「フィコンパ」4mg群、8mg群、12mg群 vs プラセボ群 = 22.7%、28.6%、42.2% vs 5.7%)、傾眠(同 15.9%、17.7%、17.8% vs 13.1%)でした。 |
4. 332試験の概要2
※左右にスクロールできます
| 試験名称 | : | 強直間代発作を有する難治性全般てんかん患者様を対象とした他剤併用時における「フィコンパ」の有効性及び安全性を評価する多施設共同無作為化二重盲検プラセボ対照並行群間比較試験 |
|---|---|---|
| 対象 | : | 1∼3種類の抗てんかん剤治療を受けている強直間代発作を有する12歳以上の患者様164名 |
| 投与法 | : | プラセボ対照、「フィコンパ」を1日1回経口投与、治療漸増期に8mg/日まで漸増し、治療維持期に8mg/日投与 |
| 治療期間 | : | 観察期(スクリーニング期及び観察期) 最長12週間 治療期(治療漸増期4週間及び治療維持期13週間) 17週間 継続投与期 38週間以上 |
| 実施地域 | : | 米国、欧州、日本、アジア |
| 主要評価項目 | : | 強直間代発作頻度変化率(28日間あたりの強直間代発作頻度の観察期からの変化率) |
| 結果 |
|
|
| 主な有害事象 | : | 「フィコンパ」群で10%より発生頻度が高く、かつプラセボ群より発生頻度が高い一般的な有害事象は、浮動性めまい(「フィコンパ」群 vs プラセボ群 = 32.1% vs 6.1%)、疲労(同 14.8% vs 6.1%)、頭痛(同 12.3% vs 9.8%)、傾眠(同 11.1% vs 3.7%)、易刺激性(同 11.1% vs 2.4%)でした。 |
5. AMPA受容体について
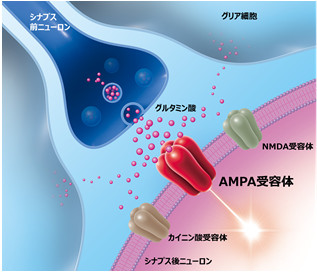
神経細胞はシナプスを介して情報伝達を行っています。神経細胞に電気信号が伝達されると、シナプスにある小胞から神経伝達物質がシナプス間隙に分泌されます。神経伝達物質が次の神経細胞の細胞膜にある受容体に結合すると、電気信号が生じて情報が伝達されます。
グルタミン酸は、中枢神経系で広く利用されている興奮性神経伝達物質です。グルタミン酸受容体には、AMPA受容体やNMDA受容体、カイニン酸受容体などが知られています。AMPA受容体 は、非常に早い興奮性神経伝達を行う受容体で、ほとんどの中枢神経細胞に発現しており、てんかん発作の発生及び伝播において中心的な役割を果たしていると考えられています。
6. てんかんについて
てんかんの患者様数は、日本で約100万人、米国で約290万人、欧州で約600万人、世界中で約6,000万人と報告されています。てんかん患者様の約30%が既存の抗てんかん剤では発作を十分にコントロールできておらず3、アンメット・メディカル・ニーズの高い疾患です。
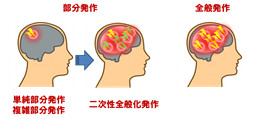
てんかんは、発作のタイプによって、てんかん全体の約6割を占める部分てんかんと、約4割を占める全般てんかんに大別されます。部分てんかんの発作では、脳の電気信号の異常が一部分に限定されています。部分発作の中には、異常が二次的に脳全体に広がり、全般性の発作になるものもあります(二次性全般化発作)。全般てんかんの発作では、電気信号の異常が脳全体に起こり、発作直後から意識がなくなったり、全身に症状が現れたりします。
全般てんかん患者様の強直間代発作は全般てんかんにおける最も一般的かつ重篤な発作型の一つであり、全般てんかんの約6割、てんかん全体においても約2割を占めます5。
強直間代発作は、突然の転倒による重篤なけがの恐れがあるほか、その発作頻度は「てんかん患者の予期せぬ突然死(SUDEP: Sudden Unexpected Death in Epilepsy)」の最も重要な危険因子とされ4、てんかんの中でも極めて重篤な発作型の一つです。強直間代発作は、多くの患者様でなんら予告症状なしに意識喪失を生じ、急激な強直性筋収縮による転倒に次いで、間代性けいれんを経て、筋弛緩し、意識障害に至る重篤な経過をたどることから、日常生活上の支障が大きいことが知られています。発作は数分で治まり、しばらく意識不鮮明やもうろう状態あるいは睡眠に移行した後、正常に戻るのが一般的な経過です。
- 1
Nishida T, et al. “A randomized double-blind, placebo-controlled study to evaluate the efficacy and safety of perampanel as adjunctive therapy in patients with refractory partial-onset seizures from the Asia-Pacific region” Abstract. 69th American Epilepsy Society (AES) Annual Meeting, 2015; 3.256
- 2
French JA, et al. “Perampanel for tonic-clonic seizures in idiopathic generalized epilepsy” Neurology 2015; 85, 950–957
- 3
“The Epilepsies and Seizures: Hope Through Research. What are the epilepsies?” National Institute of Neurological Disorders and Stroke, accessed March 10, 2016, http://www.ninds.nih.gov/disorders/epilepsy/detail_epilepsy.htm#230253109
- 4
Shorvon S, Tomson T. “Sudden unexpected death in epilepsy.” Lancet, 2011; 378:2028-2038
- 5
Hauser WA, et al. Epilepsia, 34(3):453-468,1993
