- 研究開発
- 製品情報
- 印刷用
- 2023年5月17日
エーザイ株式会社(本社:東京都、代表執行役CEO:内藤晴夫)は、このたび、アルツハイマー病(AD)による軽度認知障害(MCI)および軽度AD(総称して早期ADと定義)当事者様に対する抗アミロイドβ(Aβ)プロトフィブリル*抗体レカネマブ(一般名、米国ブランド名「LEQEMBITM」)の日本の医療システム下における社会的価値をシミュレーションした結果が査読学術専門誌Neurology and Therapy誌に掲載されたことをお知らせします。本論文では、レカネマブによる治療が、日本において、早期AD当事者様や介護者に健康アウトカムや生活の質(QOL)の向上とともに、経済的負担の軽減をもたらす可能性が示唆されたと結論付けています。
本シミュレーションは、アミロイド病理を有する早期AD当事者様に対するレカネマブの有効性と安全性を評価した臨床第Ⅲ相Clarity AD試験のデータに加え、日本の医療環境を考慮して日本の疫学データや介護実態調査等の政府統計、その他の先行研究論文を用い、直接的なケアコスト(外来・入院サービス、介護・在宅医療サービス、当事者様の薬剤費、その他介入コストなど)に焦点を当てた医療支払者観点ならびに社会的観点(直接的なケアコストに加えて家族介護によるインフォーマル・ケアコストなどを含む社会的コスト)から、学術的に検証された疾患シミュレーション・モデル(AD Archimedes Condition Event simulation:AD ACEモデル1,2)を用いて実施しました。今回の論文では、レカネマブによる健康アウトカムの改善効果と費用削減効果の双方を統合し、レカネマブの年間価値を推計しました。なお、健康アウトカム改善効果については、米国での先行研究や、米国ICER(Institute for Clinical and Economic Review)によるベンチマーク価格の推定プロセスを参考に推計しました。
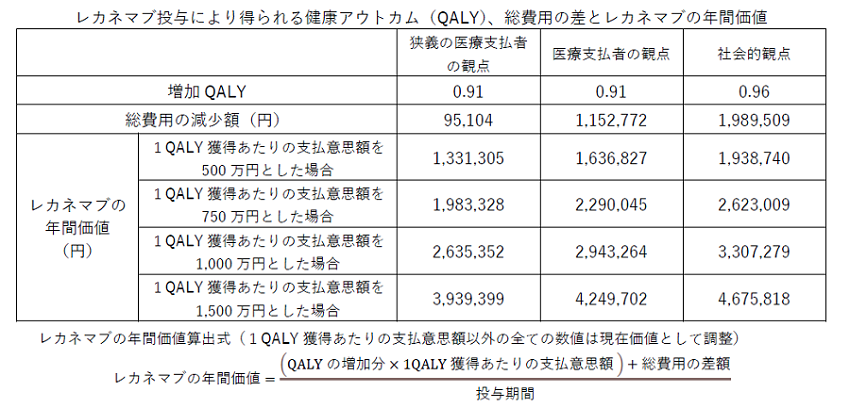
その結果、標準治療**(SoC:standard of care)に加えレカネマブ投与を行った群(レカネマブ群)の獲得質調整生存年***(QALY:Quality-Adjusted Life Year)は、SoCのみ行った群(SoC群)と比較して、狭義の医療支払者(医療費のみ)で0.91増加し(SoC群:6.12、レカネマブ群:7.03)、医療支払者の観点(医療費と公的介護費)でも0.91増加し(SoC群:6.12、レカネマブ群:7.03)、社会的観点では0.96増加する(SoC群:5.78、レカネマブ群:6.74)と推計されました。また、レカネマブ群の総費用は、SoC群と比較して、狭義の医療支払者の観点で9万5,104円の減少(Soc群:279万3,491円、レカネマブ群:269万8,387円)、医療支払者の観点では115万2,772円の減少(Soc群:1,138万1,044円、レカネマブ群:1,022万8,272円)となり、さらに社会的観点に基づく評価では198万9,509円の減少(SoC群:2,448万2,321円、レカネマブ群:2,249万2,811円)となりました。また、本シミュレーションで得られたレカネマブの平均投与期間は3.68年でした。
上記の要素を踏まえつつ、日本の医療システム下における1QALY獲得あたりの支払意思額を500万円-1,500万円とした場合のレカネマブの年間価値は、狭義の医療支払者の観点で133万1,305円-393万9,399円、医療支払者の観点で163万6,827円-424万9,702円、社会的観点に基づく評価で193万8,740円-467万5,818円と試算されました。なお、1QALY獲得あたりの支払意思額については、高度ADでは一人当たりの国内総生産(GDP)の5倍にすることが適切であると提唱する論文も有り3、またAD以外の一般的な疾患では国際的に見て支払意思額の設定に際しては一人当たりGDPの1-3倍に相当するという考え方も考慮して、本論文では1QALY獲得あたりの支払意思額は1,500万円が妥当であると判断しています。また、ADは医療費のみならず公的介護費、さらには家族介護も含めた見えない負担が膨大なものとなっていることから社会的価値を認識することが重要であり、本論文において、これらの社会的観点に基づくレカネマブの年間価値は最大467万5,818円になることが示されています。
エーザイ株式会社の常務執行役であり、チーフガバメントリレーションズオフィサー(兼)グローバルバリュー&アクセス担当である赤名正臣は、「日本における公的介護保険財政の約50%はADによる介護費用のために支出されており(2018年の公的介護保険財政:9兆6,266億円、AD公的介護費用:4兆7,832億円)、ADは医療費だけでなく介護財政に大きな影響を与えるとともに、そのコストは病態ステージの進行によって大きく増加し、MCIと高度認知症を比較すると医療費は約2倍、介護費は約10倍に大きく増加することが推定されています4。今回のシミュレーションによって、日本において、レカネマブによる治療は当事者様に病態進行の遅延をもたらし、介護者や社会全体に対して大きなインパクトを与えることが示されました。本論文は、ステークホルダーズの皆様が日本におけるレカネマブの潜在的な臨床的・社会経済的価値について理解を深め、製薬企業によるイノベーションの評価について議論するための重要な情報となると考えています。当社は、治療薬を待ち望む早期AD当事者様にレカネマブをお届けするべく、引き続き透明性高く、迅速にデータと情報を公表してまいります」と述べています。
本論文の筆頭著者である、公立大学法人横浜市立大学 医学群准教授、東京大学大学院 薬学系研究科 医薬政策学 客員准教授の五十嵐中先生は、「本論文は、米国での手法を踏襲しつつ、日本特有の条件を加味して薬剤のもたらす社会的価値を推定したものです。認知症に限らず薬剤の価値評価については、有効性・安全性、治療費以外に、様々な側面、例えば仕事への影響や家族・医療者の負担軽減度なども考慮するべきと考えています」と述べています。
レカネマブについては、当社が開発および薬事申請をグローバルに主導し、当社の最終意思決定権のもとで、当社とバイオジェン・インクは共同商業化・共同販促を行います。
* プロトフィブリルは、75-5000Kdの可溶性Aβ凝集体です5。
** 生活習慣の改善と症状に対する薬物治療
*** 質調整生存年(QALY)は、健康アウトカムの価値を示す指標です。健康は生存年(=量)と生命の質(QOL)の関数であるため、これらの価値を1つの指標数値にまとめる試みとしてQALYが開発されました。1QALYは、完全に健康な状態での1年間に相当します。QOLスコアは、1(完全な健康)から0(死亡)で示されます。例えば、新規治療と既存治療でいずれも生存年が3年延長し、新規治療ではQOLが0.7の状態(QALY=2.1)を維持できる一方で、既存治療ではQOLがより低く、0.5の状態(QALY=1.5)だった場合には、新規治療の増分QALYは0.6となります(QALY=QOLスコアx生存年)。
以上
参考文献
1 Tahami Monfared AA, Tafazzoli A, Ye W, Chavan A, Zhang Q. Long-Term Health Outcomes of Lecanemab in Patients with Early Alzheimer’s Disease Using Simulation Modeling. Neurology and therapy. 2022;11(2):863-80.
2 Tahami Monfared AA, Tafazzoli A, Chavan A, Ye W, Zhang Q. The Potential Economic Value of Lecanemab in Patients with Early Alzheimer’s Disease Using Simulation Modeling. Neurology and Therapy. 2022;11(3):1285-307.
3 Lakdawalla DN, Phelps CE. Health technology assessment with risk aversion in health. J Health Econ. 2020;72:102346. doi: 10.1016/j.jhealeco.2020.102346
4 S. Ikeda, M. Mimura, M. Ikeda, K .Wada-Isoe, M. Azuma, S. Inoue, K. Tomita. Economic Burden of Alzheimer’s Disease Dementia in Japan. Journal of Alzheimer’s Disease 81(2021)309-319
5 Söderberg, L., Johannesson, M., Nygren, P. et al. Lecanemab, Aducanumab, and Gantenerumab — Binding Profiles to Different Forms of Amyloid-Beta Might Explain Efficacy and Side Effects in Clinical Trials for Alzheimer’s Disease. Neurotherapeutics (2022).
<参考資料>
- 1. レカネマブ(一般名、米国ブランド名「LEQEMBITM」)について
レカネマブは、BioArctic AB(本社:スウェーデン、以下 バイオアークティック)とエーザイの共同研究から得られた、アミロイドベータ(Aβ)の可溶性(プロトフィブリル)および不溶性凝集体に対するヒト化IgG1モノクローナル抗体です。米国において、「LEQEMBI」は、2023年1月6日に米国食品医薬品局(FDA)より迅速承認を取得しました。「LEQEMBI」の適応症はアルツハイマー病(AD)の治療です。「LEQEMBI」による治療は、臨床試験と同様、ADによる軽度認知障害または軽度認知症の当事者様において開始する必要があります。これらの病期よりも早期または後期段階での治療開始に関する安全性と有効性のデータはありません。本適応症は、「LEQEMBI」がADの特徴である脳内に蓄積したAβプラークの減少効果を示した臨床第Ⅱ相試験の結果に基づき、迅速承認の下で承認されています。本迅速承認の要件として、検証試験による臨床的有用性の確認が必要となります。
米国における処方情報はこちらから入手できます。
米国において、2023年1月6日に迅速承認からフル承認への変更に向けた生物製剤承認一部変更申請(supplemental Biologics License Application:sBLA)をFDAに提出し、3月3日に受理されました。本申請は優先審査に指定され、PDUFA(Prescription Drugs User Fee Act)アクションデート(審査終了目標日)は2023年7月6日に設定されました。本申請について、FDAは6月9日に諮問委員会を予定しています。日本において、当社は、2023年1月16日に、独立行政法人医薬品医療機器総合機構(PMDA)に製造販売承認申請を行い、1月26日に厚生労働省より優先審査に指定されました。本申請においては、審査期間の短縮をめざし医薬品事前評価相談制度を活用しています。欧州においても、2023年1月9日に欧州医薬品庁(EMA)に販売承認申請(MAA)を提出し、1月26日に受理されました。中国においては、2022年12月に国家薬品監督管理局(NMPA)に生物ライセンス申請(BLA)のデータ提出を開始し、2023年2月27日に優先審査に指定されました。カナダにおいては、2023年3月31日にカナダ保健省(Health Canada)に新薬承認申請を行い、同年5月15日に受理されました。
レカネマブの皮下注射によるバイオアベイラビリティ試験は終了し、Clarity AD試験OLEにおいて皮下投与の評価が進行中です。
2020年7月から、臨床症状は正常で、ADのより早期ステージにあたる脳内Aβ蓄積が境界域レベルおよび陽性レベルのプレクリニカルADを対象とした臨床第Ⅲ相試験(AHEAD 3-45試験)を米国のADおよび関連する認知症の学術的臨床試験のための基盤を提供するAlzheimer's Clinical Trials Consortium(ACTC)とのパブリック・プライベート・パートナーシップ(PPP)で行っています。ACTCは、National Institutes of Health、National Institute on Agingによる資金提供を受けています。また、2022年1月から、セントルイス・ワシントン大学医学部(米国ミズーリ州セントルイス)が主導する優性遺伝アルツハイマーネットワーク試験ユニット(Dominantly Inherited Alzheimer Network Trials Unit、以下 DIAN-TU)が実施する優性遺伝アルツハイマー病(DIAD)に対する臨床試験(Tau NexGen試験)が進行中です。
2. エーザイとバイオジェンによるAD領域の提携について
エーザイとバイオジェンは、AD治療剤の共同開発・共同販売に関する提携を2014年から行っています。レカネマブについて、エーザイは、開発および薬事申請をグローバルに主導し、エーザイの最終意思決定権のもとで、エーザイとバイオジェンが共同商業化・共同販促を行います。
3. エーザイとバイオアークティックによるAD領域の提携について
2005年以来、エーザイとバイオアークティックはAD治療薬の開発と商業化に関して長期的な協力関係を築いてきました。エーザイは、レカネマブについて、2007年12月にバイオアークティックとのライセンス契約により、全世界におけるADを対象とした研究・開発・製造・販売に関する権利を取得しています。2015年5月にレカネマブのバックアップ抗体の開発・商業化契約を締結しました。
当社のニュースリリースは、企業情報の開示を目的としており、医療用医薬品や開発品のプロモーションや広告、医学的なアドバイスを目的とするものではありません。なお、ニュースリリースに記載している情報は発表日現在のものです。