- 印刷用
- 2022年9月12日
エーザイ株式会社(本社:東京都、代表執行役CEO:内藤晴夫)は、2022年9月9日から13日までフランスパリおよびバーチャルのハイブリッド形式で開催中の「欧州臨床腫瘍学会(European Society for Medical Oncology:ESMO)年次総会」において、エリブリンメシル 酸塩(製品名:「ハラヴェン®」、以下 エリブリン)の有効性を他の化学療法(治験医師選択療法、カペシタビンおよびビノレルビン)と比較評価した3つのピボタル無作為化臨床第III相試験(それぞれEMBRACE試験/305試験、301試験、304試験)について、HER2低発現または陰性の転移性乳がん患者様を対象とした事後解析結果に関する最新の知見(ポスター抄録番号:259P)を発表したことをお知らせします。
HER2低発現乳がんサブタイプは、これまでHER2陰性に分類されてきた乳がんのなかで、免疫組織化学染色(Immunohistochemistry: IHC)測定法およびin situハイブリダイゼーション(ISH)測定法に基づき、新しく定義された腫瘍分類です。HER2低発現腫瘍は、HER2タンパク質の発現量が低く、HER2陽性と判断されない腫瘍です。「HER2低発現」はIHC測定法におけるスコアが1+、あるいはIHCスコアが2かつISH測定法で陰性である場合と定義されています。2022年に米国で新たに女性乳がんと診断されると推計される約28万8000人のうち1、約80~85%がHER2陰性サブタイプに属すると考えられていましたが、現在は、これらの患者様のうち、約60%がHER2低発現サブタイプに属すると推定されています2。
当社チーフサイエンティフィックオフィサーである常務執行役大和隆志博士は、「本事後解析では、HER2低発現の転移性乳がん患者様におけるアウトカムが、3つのピボタル臨床第Ⅲ相試験の結果と一貫性があることが示されました。オンコロジーのサイエンスコミュニティにおいて転移性乳がんに対する理解が深まる中、我々は新たな状況における既存治療法の役割評価を継続して行い、医療専門家のナレッジ拡大に貢献していくことが重要です」と述べています。
事後解析結果
本事後解析には、アントラサイクリンおよびタキサンを含む化学療法の治療歴がある(301試験では2レジメン以下、304試験およびEMBRACE 試験/305試験では2-5レジメン)局所再発または転移性乳がんを対象としたエリブリンと治験医師選択療法の比較試験(NCT00388726、EMBRACE 試験/305試験)、エリブリンとカペシタビンの比較試験(NCT00337103、301試験)、エリブリンとビノレルビンの比較試験(NCT02225470、304試験)のデータが含まれます。EMBRACE 試験/305試験、301試験および304試験において合計1,589名の適格な患者様が登録され、ベースラインの特徴は、それぞれの試験における治療群間で概ね均一でした。
これらの試験において、全生存期間(Overall Survival: OS)中央値、無増悪生存期間(Progression-Free Survival: PFS)中央値、奏効率(Objective Response Rate: ORR)が評価されました。PFSとORRは、独立画像判定により、固形がんに対する腫瘍径の変化を効果判定に用いる評価基準であるRECISTを用いて評価されました(EMBRACE 試験/305試験および301試験ではRECISTv1.0、304試験では同v1.1を使用)。ORRは、評価可能な患者様集団(EMBRACE 試験/305試験)およびIntention-To-Treat(ITT)集団(301試験および304試験)において測定されました。
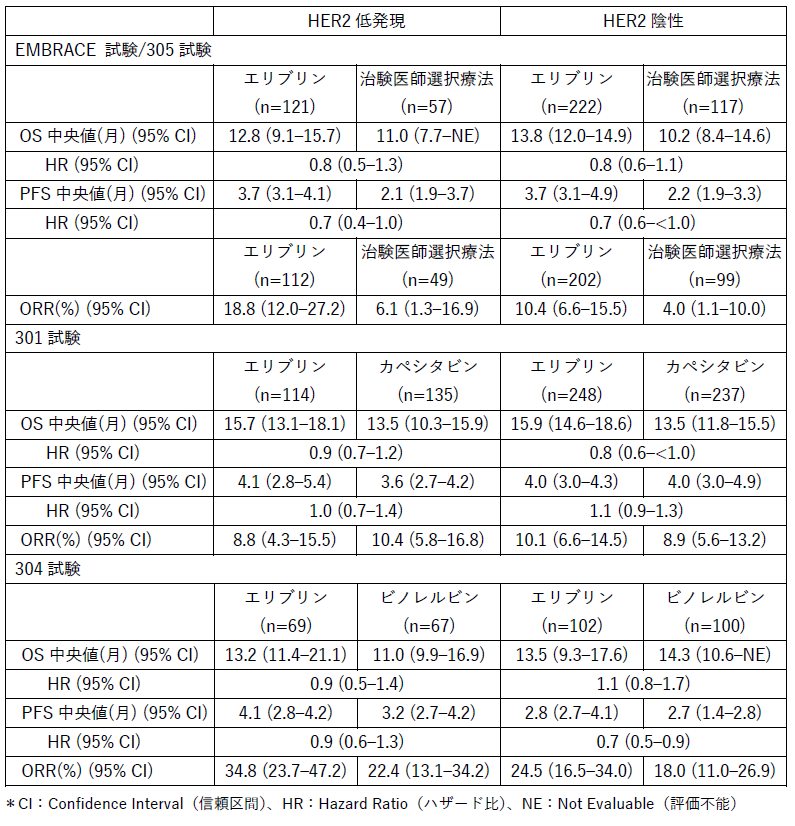
本事後解析では、EMBRACE 試験/305試験、301試験および304試験の各試験において、HER2低発現または陰性の患者様集団のOS、PFS、ORRは、エリブリン投与群全体と概ね同等でした3,4,5。各試験のHER2低発現および陰性の患者様に対する有効性の結果は以下の表のとおりです。
<参考資料>
- 1. 乳がんについて
転移性乳がんは、乳房以外の身体の他の部分に広がっている進行期のがんです。乳がんの新規罹患者様数は、2020年に世界で約226万1千人以上と推定され、68万4千人以上が亡くなったと推定されています6。日本では、2020年に9万2千人以上が新たに診断され、1万7千人以上が亡くなったと推定されています7。米国では、2022年には約28万8千人の女性が乳がんと診断され、4万3千人以上が亡くなると推定されています1。早期乳がん患者様の30%が転移性乳がんへと進行し8、乳がん女性の約6%は診断時に転移性と診断されるとされています9。転移性乳がんは、非転移性乳がんと比較して予後不良です。女性転移性乳がんの5年相対生存率は28%です10。
- 2. エリブリンメシル酸塩(製品名:「ハラヴェン」)について
エリブリンは、自社創製の新規の作用機序を有するハリコンドリン系の微小管ダイナミクス阻害剤です。海洋生物クロイソカイメン(Halichondria okadai )から抽出された天然物ハリコンドリンBの全合成類縁化合物であり、微小管の伸長(重合)を阻害・抑制することによる、細胞分裂の停止作用を有しています。加えて、非臨床研究において、腫瘍の血流循環を改善すること11、乳がん細胞の上皮細胞化を誘導すること、乳がん細胞の転移能を減少させる12など、がん微小環境におけるユニークな作用を有することが知られています。
エリブリンが取得している適応は以下の通りです。
・乳がんに係る適応(日本、米国、欧州、中国・アジアなど80カ国以上で承認を取得)
日本:手術不能又は再発乳癌
米国:アントラサイクリン系及びタキサン系抗がん剤を含む少なくとも2レジメンのがん化学療法による前治療歴のある転移性乳がん
欧州:1レジメン以上の前治療歴のある局所進行性・転移性乳がん(術後または再発後にアントラサイクリン系及びタキサン系抗がん剤による治療歴を有すること)
・悪性軟部腫瘍に係る適応(日本、米国、欧州、アジアなど80カ国以上で承認を取得)
日本:悪性軟部腫瘍
米国:アントラサイクリン系抗がん剤治療を含む化学療法の前治療歴のある手術不能または転移性の脂肪肉腫
欧州:進行または転移性で、アントラサイクリン系抗がん剤治療(不適な場合を除く)を含む化学療法の前治療歴のある手術不能な成人の脂肪肉腫
1 National Institutes of Health, National Cancer Institute website, “Cancer Stat Facts: Female Breast Cancer”:
https://seer.cancer.gov/statfacts/html/breast.html
2 U.S. FOOD & DRUG ADMINISTRATION website, “FDA Approves First Targeted Therapy for HER2-Low Breast Cancer”:
3 Cortés J et al. Lancet. 2011 Mar 12;377(9769):914-23.
https://www.thelancet.com/action/showPdf?pii=S0140-6736%2811%2960070-6
4 Kaufman PA et al. J Clin Oncol. 2015 Feb 20;33(6):594-601.
https://ascopubs.org/doi/pdfdirect/10.1200/JCO.2013.52.4892
5 Yuan P et al. Eur J Cancer. 2019;112:57-65.
https://www.ejcancer.com/article/S0959-8049(19)30139-X/pdf
6 International Agency for Research on Cancer, World Health Organization. “Breast Fact Sheet.” Cancer Today, 2020.:
https://gco.iarc.fr/today/data/factsheets/cancers/20-Breast-fact-sheet.pdf
7 International Agency for Research on Cancer, World Health Organization. “Japan Fact Sheet.” Cancer Today, 2020.:
https://gco.iarc.fr/today/data/factsheets/populations/392-japan-fact-sheets.pdf
8 BREASTCANCER ORG website, “Metastatic Breast Cancer”:
https://www.breastcancer.org/types/metastatic
9 American Cancer Society. “Breast Cancer Facts & Figures 2019-2020”:
10 Cancet.Net website. “Breast cancer – Metastatic: Statistics”:
https://www.cancer.net/cancer-types/breast-cancer-metastatic/statistics
11 Funahashi Y et al., Cancer Sci., 2014; 105, 1334-1342
https://onlinelibrary.wiley.com/doi/epdf/10.1111/cas.12488
12 Yoshida T et al., Br J Cancer, 2014; 110, 1497-1505
https://www.nature.com/articles/bjc201480
当社のニュースリリースは、企業情報の開示を目的としており、医療用医薬品や開発品のプロモーションや広告、医学的なアドバイスを目的とするものではありません。なお、ニュースリリースに記載している情報は発表日現在のものです。