- 印刷用
- 2017年7月27日
エーザイ株式会社(本社:東京都、代表執行役CEO:内藤晴夫)は、米国子会社のエーザイ・インクが、2017年7月26日(米国時間)、自社創製の抗てんかん剤「Fycompa®」(一般名:ペランパネル、日本製品名「フィコンパ®」)について、米国食品医薬品局(FDA)より、12歳以上のてんかん患者様の部分発作(二次性全般化発作を含む)に対する単剤療法での使用に関する承認を取得したことをお知らせします。
2016年9月に発出されたFDAの抗てんかん剤の単剤療法での使用に関する規制方式1では、部分てんかんの併用療法として承認された薬剤における安全性と効果が、単剤療法でも同様に得られると推定される場合、当該薬剤を単剤療法として使用することが可能となりました。「Fycompa」は、本規制方式に基づいて、部分てんかんにおける単剤療法の承認を取得した初めての薬剤となります。
「Fycompa」は、当社の筑波研究所で創製されたファースト・イン・クラスの抗てんかん剤です。グルタミン酸によるシナプス後AMPA受容体の活性化を高選択的かつ非競合的に阻害する唯一の薬剤で、神経の過興奮を抑制します。米国においては、これまで12歳以上のてんかん患者様の部分発作(二次性全般化発作を含む)および強直間代発作に対する併用療法の適応で承認を取得していました。今回の部分てんかんの単剤療法の承認により、米国では、12歳以上のすべての部分てんかんを有する患者様に投与可能となります。
米国におけるてんかん患者様数は290万人と報告されており、てんかんの約6割は、部分てんかんに分類されています2。当社は、神経領域を重点疾患領域と位置づけており、米国における「Fycompa」の部分てんかん単剤療法による新たな治療選択肢の提供を機に、てんかんの患者様とそのご家族の多様なニーズの充足とベネフィット向上により一層貢献してまいります。
以上
<参考資料>
1. 「Fycompa」(一般名:ペランパネル、日本製品名「フィコンパ」)について
「Fycompa」は、当社が創製したファースト・イン・クラスの抗てんかん剤です。てんかん発作は、神経伝達物質であるグルタミン酸により誘発されることが報告されており、本剤は、グルタミン酸によるシナプス後AMPA受容体の活性化を阻害し、神経の過興奮を抑制する高選択、非競合AMPA受容体拮抗剤です。「Fycompa」は1日1回就寝前に経口投与するタイプの錠剤です。さらに、新たな剤形として経口懸濁液の承認を米国で取得し、販売しています。
本剤は、12歳以上のてんかん患者様の部分発作(二次性全般化発作を含む)に対する併用療法を適応として、日本、米国、欧州など55カ国以上で承認を取得しています。さらに本剤は、全般てんかん患者様の強直間代発作に対する併用療法について、日本、米国、欧州など45カ国以上で承認を取得しています。
今回の追加承認取得により、米国での効能・効果は、12歳以上のてんかん患者様の「部分発作(二次性全般化発作を含む)」および「全般てんかんの強直間代発作に対する併用療法」となります。
日本では、「他の抗てんかん薬で十分な効果が認められないてんかん患者の部分発作(二次性全般化発作を含む)および強直間代発作に対する抗てんかん薬との併用療法」の適応で承認を取得しています。
本剤について、部分発作または強直間代発作を有する小児てんかん患者様を対象としたグローバル臨床第Ⅲ相試験、レノックス・ガストー症候群に伴うてんかん発作を有する患者様を対象としたグローバル臨床第Ⅲ相試験を実施しています。また、日本では、部分てんかん単剤療法に対する臨床第Ⅲ相試験を実施しています。
米国での「Fycompa」の重要な安全性情報を含む本剤に関する詳細はウェブサイトをご参照ください。
2. てんかんの治療について
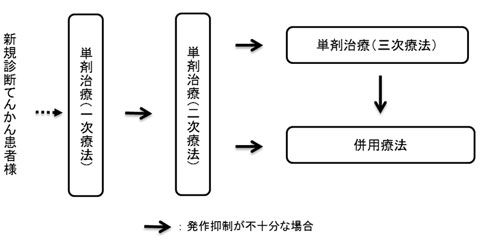
てんかん患者様の治療ゴールはてんかん発作の抑制です。てんかんと診断されると抗てんかん剤の単剤療法で治療を行いますが、発作抑制効果が十分でない場合には、他の単剤療法あるいは併用療法に切り替えます。
- 1FDA Communication. Reference ID: 3985169. September 13, 2016.
- 2Hauser WA, et al. Epilepsia, 34(3):453-468,1993
