- 印刷用
- 2017年5月31日
エーザイ株式会社(本社:東京都、代表執行役CEO:内藤晴夫)は、このたび、マサチューセッツ工科大学とハーバード大学との共同研究施設であるブロード研究所(Broad Institute、所在地:米国マサチューセッツ州ケンブリッジ)と、2016年に共同研究チームが見出した創薬ターゲットに基づく新規抗マラリア薬開発に向けて、新たな共同研究契約を締結しましたのでお知らせします。
当社とブロード研究所の抗マラリア薬の共同研究プログラムは、2014年9月に締結した契約により開始され、ブロード研究所のライブラリーからスクリーニングされた一連の化合物から、有望な候補化合物群を見出し、最適化しました。これら候補化合物群は、既存の抗マラリア薬の作用機序とは全く異なる蛋白合成酵素(フェニルアラニンt-RNA合成酵素)阻害作用を持ち、試験管内および動物感染モデルを使った実験で、血液期、肝臓期および伝播期のマラリア原虫に対して、強い活性を示しました。本成果は、2016年9月に発行された科学雑誌Nature誌に掲載されました1。
マラリアは、蚊に媒介されてマラリア原虫が人に感染する寄生虫症です。致死性が高く、世界保健機関(WHO)によると、2015年のマラリアによる推定死亡者数は約43万人で、その多くがアフリカの子供達であると報告されています2。現在の抗マラリア薬のほとんどは、赤血球の中でマラリア原虫が増殖する血液期に作用するため、肝臓期、伝播期を含む原虫のすべてのライフステージで作用する薬剤の開発が必要とされています。また、マラリア原虫は、抗マラリア薬に対して耐性を持つようになるため、新規作用機序を持つ薬剤の開発も喫緊の課題となっています。
本契約において、ブロード研究所のメディシナルケミストリーおよび当社の薬剤開発に関する知見を活用し、今までのプロジェクトの成果をベースに、より優れた特徴を持つ新規化合物群の創製をめざします。なお、本契約において、当社は、最適化合物の選択後に、開発に関する独占的ライセンスを受けるオプション権を保有しています。
当社代表執行役CEOである内藤晴夫は、「ブロード研究所との共同研究プログラムの順調な進展が、新規抗マラリア薬を必要としている数百万人という患者様への貢献につながることを期待しています。エーザイは、これらグローバルヘルスへの貢献を、我々のミッションであるとともに、健康で豊かな中間所得層を生み出すための長期的な投資と位置づけ、積極的に取り組んでいます。」と述べています。
ブロード研究所の設立メンバーであり、医薬研究やケミカルバイオロジー分野の第一人者、さらに共同研究チームリーダーであるStuart L. Schreiber教授は、「本プロジェクトが成功すれば、既存の抗マラリア薬とは全く異なる新規作用機序を持つ薬になります。既存の抗マラリア薬は上市から10年以上経っており、薬剤耐性の出現が急速に進んでいます。エーザイは、非営利学術研究機関と共同で、新しい有望な治療アプローチを探索することに注力しており、この取り組みが開発途上国の数十万人の子供達の命を脅かす疾患の克服につながることを期待しています。」と述べています。
なお、この共同研究プログラムは、公益社団法人グローバルヘルス技術振興基金(GHIT Fund)の助成金交付対象として採択されました。
当社はヒューマン・ヘルスケア(hhc)理念のもと、政府や国際機関、非営利民間団体などと積極的にパートナーシップを締結して、マラリアや結核、顧みられない熱帯病に苦しんでいる患者様とそのご家族に貢献する新たな治療法の早期開発をめざしてまいります。
以上
<参考資料>
1. ブロード研究所について
ブロード研究所(Broad Institute)は、ハーバード大学とマサチューセッツ工科大学の共同研究施設です。ゲノム医学における世界有数の研究機関であり、感染症を含む様々な疾患関連遺伝子を体系的に解明するための研究に、世界に先駆けて取り組んでいます。詳細は、www.broadinstitute.orgをご参照ください。
2. 公益社団法人グローバルヘルス技術振興基金(GHIT Fund)について
公益社団法人グローバルヘルス技術振興基金(GHIT Fund)は、グローバルヘルス分野の製品開発に特化した世界初の官民パートナーシップとして、日本政府(外務省、厚生労働省)、製薬企業などの民間企業、ビル&メリンダ・ゲイツ財団、ウェルカム・トラスト、国連開発計画が参画する、国際的な非営利組織です。GHIT Fundは2013年4月に設立され、世界の最貧困層の健康を脅かす感染症と闘うために、製品開発パートナーシップへの投資ならびに、ポートフォリオマネジメントを行っています。開発途上国に蔓延するHIV/AIDS、マラリア、結核、顧みられない熱帯病(NTDs)などの感染症の制圧を目指し、日本と海外の研究機関の連携促進を行い、製品開発パートナーシップへの投資を通じて新薬開発を推進しています。詳しくは、http://www.ghitfund.orgをご覧ください。
3. マラリアについて
マラリアは、マラリア原虫を持つ蚊に媒介されて人に感染する寄生虫症です。致死性が高く、世界保健機関(WHO)によると、2015年の推定マラリア感染者数は2.1億人であり、推定で年間約43万人が死亡しており、その多くがアフリカの子供達であると報告されています2。
下図に示すように、蚊による吸血時にヒトの体内に入ったマラリア原虫(①)は、まず肝細胞に感染し増殖(②、③:肝臓期)した後、血液中に移行し赤血球の中で増殖(④)します。その後、赤血球を破壊して次の赤血球に浸入するというサイクル(④→⑤→⑥→④→・・・:血液期)を繰り返します。マラリアの症状が出るのは赤血球内のサイクルにおいてであり、マラリアの治療ではこのステージの原虫に作用する薬剤を用います。ただし、三日熱マラリア原虫などの原虫の一部は、感染した肝細胞(②)で増殖せずに休眠することがあり、血中の原虫(④∼⑥)を駆虫した後に、肝細胞において休眠していた原虫が何らかの刺激により増殖を開始することが知られています(再発)。
また、赤血球で増殖する原虫のほとんどは性別のない無性世代ですが、蚊に吸血された後、これら無性世代の原虫は蚊の体内で死んでしまいます。一方で、赤血球中で雄と雌に性分化した一部の原虫(⑥:伝播期)は、蚊の体内で生殖(⑦∼⑧)することができます(伝播)。従って、雄と雌に性分化した原虫を、ヒトの血中で駆虫することができれば、蚊によるマラリアの伝播を防ぐことが期待されます。
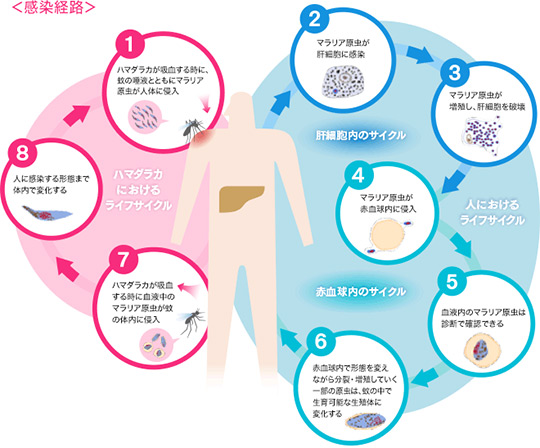
エーザイ ATM ナビゲーターより(https://www.eisai.co.jp/sustainability/atm/index.html)
4. マラリアの治療薬について
現在の抗マラリア薬のほとんどは、赤血球の中でマラリア原虫が増殖する血液期に作用します。肝臓期や伝播期の原虫はマラリア症状を起こすことはありませんが、肝臓期から血液期への移行に伴う発症・再発や、蚊への伝播による流行を引き起こすため、これら全てのライフステージに作用する薬剤の開発が必要とされています。
さらに、マラリア原虫は、抗マラリア薬に対して耐性を持つようになるため、新規作用機序を有する薬剤の開発も喫緊の課題となっています。現在、マラリアの治療には、速効性のあるアルテミシニン系薬剤をベースとし、持続性のあるルメファントリン、アモジアキン、メフロキンなどを組み合わせた併用療法が用いられています。しかし、近年、比較的新しいアルテミシニン系薬剤に対しても耐性を持つマラリアが報告されています。
当社とブロード研究所が見出した候補化合物群は、新規作用機序を持ち、さらに前臨床試験においてマラリア原虫の血液期、肝臓期と伝播期に作用するというまれな性質が確認されており、全ライフステージに作用する薬剤につながる可能性があります。
- 1
Nobutaka Kato, et al, “Diversity-oriented synthesis yields novel multistage antimalarial inhibitors” Nature, 2016; 538, 344-349
- 2
