- 印刷用
- 2020年9月18日
エーザイ株式会社(本社:東京都、代表執行役CEO:内藤晴夫)は、このたび、自社創製の抗がん剤「ハラヴェン®」(一般名:エリブリンメシル酸塩、以下 エリブリン)の新剤形であるリポソーム製剤(E7389-LF)について、臨床第Ⅰ相試験のHER2陰性乳がん患者様を対象としたコホートに関する最新データを「欧州臨床腫瘍学会年次総会(ESMO Virtual Congress 2020)」において発表しましたのでお知らせします(抄録番号:346P)。
E7389-LFは、ハリコンドリン系の微小管ダイナミクス阻害剤であるエリブリンを、脂質二重層で構成されるリポソームに内包させた新製剤です。腫瘍組織では、不完全な血管構築により血管内皮細胞間に高分子が透過しうる間隙が存在すること、またリンパ系が発達していないことから、正常組織に比べ、リポソーム製剤を含む高分子薬剤の腫瘍への到達度および滞留度が向上するEPR(Enhanced Permeability and Retention)効果の発現が想定されており、E7389-LFでは、腫瘍組織におけるエリブリン濃度の向上が期待されます。
本発表では、前治療歴のある固形がんを対象とした非盲検臨床第Ⅰ相試験(114試験)のうちアントラサイクリン系およびタキサン系薬剤による前治療歴を有し、エリブリンによる治療歴を有さない再発乳がん(HER2陰性)コホートに登録された28人(ホルモン受容体陽性 21人、トリプルネガティブ 7人)の患者様に対するE7389-LFの有効性、安全性の結果を報告しました(データカットオフ日:2020年1月24日、無増悪生存期間、全生存期間については同年4月17日)。E7389-LFはエリブリンとして2.0 mg/m2(体表面積)が3週に1回投与され、HER2陰性乳がんコホート全体での奏効率は35.7%(95% 信頼区間 (CI): 18.6-55.9)であり、そのうちホルモン受容体陽性の患者様では42.9%(95%CI: 21.8-66.6)、トリプルネガティブの患者様では14.3%(95%CI: 0.4-57.9)でした。病勢安定率、部分奏効率、完全奏効率を合わせた病勢コントロール率は89.3%(95%CI: 71.8-97.7)でした。また、無増悪生存期間の中央値は5.7カ月(95%CI: 3.9-8.3)であり、全生存期間は中央値に到達しませんでした(95%CI: 10.3-not reached)。グレード3以上の有害事象(上位5つ)は好中球減少(67.9%)、白血球減少(42.9%)、血小板減少(32.1%)、発熱性好中球減少(25.0%)、アラニンアミノトランスフェラーゼ(ALT)増加(21.4%)であり、これまでのエリブリンの安全性プロファイルと同様でした。なお、G-CSF(顆粒球コロニー形成刺激因子)製剤であるペグフィルグラスチムの予防的投与により、発熱性好中球減少の割合が減少する傾向(投与あり:10.0%、投与なし:33.3%)が認められました。
当社は、がん領域を重点領域の一つと位置づけており、がんの「治癒」に向けた革新的な新薬創出をめざしています。最先端のがん研究から革新的な創薬を行い、がん患者様とそのご家族、さらには医療従事者の多様なニーズの充足とベネフィット向上に、より一層貢献してまいります。
以上
<参考資料>
- 1. E7389–LFについて
E7389-LFは、抗がん剤「ハラヴェン」(エリブリン)をより効率的にがん細胞に送達させることを企図してリポソームに内包させた新製剤です。日本において固形がんを対象とした臨床第Ⅰ相試験を実施中です。また、日本において小野薬品工業株式会社と共同で、固形がんを対象としたE7389-LFとニボルマブの併用療法の臨床第Ⅰb/Ⅱ相試験を実施中です。
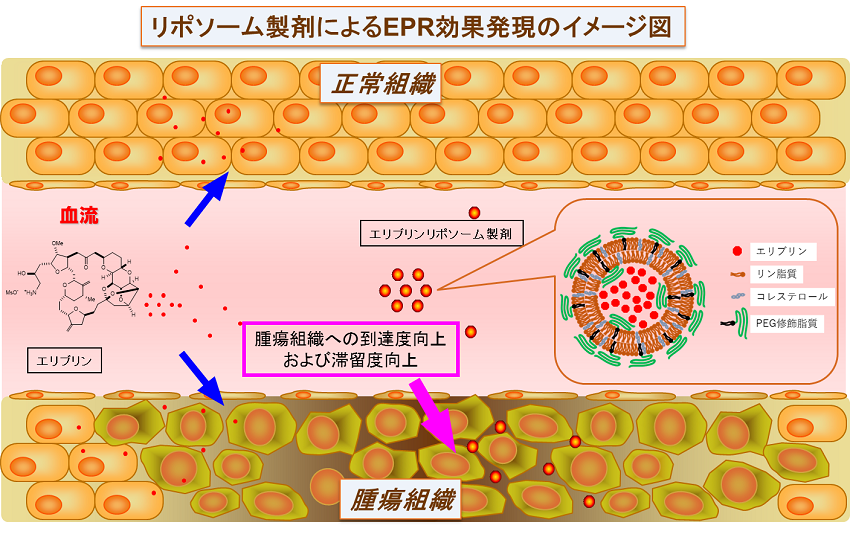
(東京理科大学西川元也先生作成の図を許諾のもと一部改編)
- 2. 「ハラヴェン」(一般名:エリブリンメシル酸塩)について
「ハラヴェン」は、新規の作用機序を有するハリコンドリン系の微小管ダイナミクス阻害剤です。海洋生物クロイソカイメン(Halichondria okadai )から抽出された天然物ハリコンドリンBの全合成類縁化合物であり、微小管の伸長(重合)を阻害・抑制することによる、細胞分裂の停止作用を有しています。加えて、非臨床研究において、腫瘍の血流循環を改善すること1、乳がん細胞の上皮細胞化を誘導すること、乳がん細胞の転移能を減少させる2など、がん微小環境におけるユニークな作用を有することが知られています。
本剤は、2010年11月に米国で乳がんに係る適応で最初の承認を取得し、これまでに日本、欧州、米州、中国、アジアなど75カ国以上で乳がんに係る適応で承認を取得しています。また、悪性軟部腫瘍に係る適応については、2016年1月に米国で最初に適応を取得したのをはじめ、日本、欧州、アジアなど65カ国以上で承認を取得しています。本剤は米国および日本において、悪性軟部腫瘍に対する希少疾病用医薬品(オーファンドラッグ)の指定を受けています。
「ハラヴェン」の米国における適応症は「アントラサイクリン系及びタキサン系抗がん剤を含む少なくとも2レジメンのがん化学療法による前治療歴のある転移性乳がん」および「アントラサイクリン系抗がん剤治療を含む化学療法の前治療歴のある手術不能または転移性の脂肪肉腫」です。日本における適応症は、「手術不能又は再発乳癌、悪性軟部腫瘍」です。欧州における適応症は、「1レジメン以上の前治療歴のある局所進行性・転移性乳がん(術後または再発後にアントラサイクリン系及びタキサン系抗がん剤による治療歴を有すること)」および「進行または転移性で、アントラサイクリン系抗がん剤治療(不適な場合を除く)を含む化学療法の前治療歴のある手術不能な成人の脂肪肉腫」です。
アントラサイクリン系およびタキサン系抗がん剤を含む前治療歴を有する進行または再発乳がんを対象とした「ハラヴェン」の2つの非盲検無作為化臨床第Ⅲ相試験(EMBRACE試験および301試験)の統合解析の結果3、全体解析において、「ハラヴェン」群はコントロール群に比べて、全生存期間(OS)を顕著に延長しました(ハザード比 0.85 [95%信頼区間(CI)=0.77–0.95]、p=0.003、OS中央値:「ハラヴェン」群15.2カ月 対 コントロール群12.8カ月)。無増悪生存期間(PFS)についても、「ハラヴェン」群はコントロール群に比べて延長しました(ハザード比0.90[95%CI=0.81-0.997]、p=0.046、PFS中央値:「ハラヴェン」群4.0カ月 対 コントロール群3.4カ月)。
奏効率について、HER2陰性群では、13.5%、そのうちホルモン受容体陽性群では14.3%、トリプルネガティブ群では、12.0%でした。HER2陰性群のPFSは、4.0カ月(中央値)でした。
統合解析における安全性プロファイルについては、各臨床試験で報告されている結果との大きな違いはありませんでした。なお、これらの臨床第Ⅲ相試験において「ハラヴェン」は、21日を1クールとして、1.4mg/m2/dayを1日目と8日目に静脈内注射により投与されました。
-
1
Funahashi Y et al., Eribulin mesylate reduces tumor microenvironment abnormality by vascular remodeling in preclinical human breast cancer models. Cancer Sci., 2014; 105, 1334-1342
-
2
Yoshida T et al., Eribulin mesilate suppresses experimental metastasis of breast cancer cells by reversing phenotype from epithelial-mesenchymal transition (EMT) to mesenchymal-epithelial transition (MET) states. Br J Cancer, 2014; 110, 1497-1505
-
3
Twelves C et al., Efficacy of eribulin in women with metastatic breast cancer: a pooled analysis of two phase 3 studies. Breast Cancer Res Treat, 2014; 148, 553-561
当社のニュースリリースは、企業情報の開示を目的としており、医療用医薬品や開発品のプロモーションや広告、医学的なアドバイスを目的とするものではありません。なお、ニュースリリースに記載している情報は発表日現在のものです。
