- 印刷用
- 2017年12月21日
エーザイ株式会社
バイオジェン・インク
エーザイ株式会社(本社:東京都、代表執行役CEO:内藤晴夫、以下 エーザイ)とバイオジェン・インク(Nasdaq: BIIB、本社:米国マサチューセッツ州ケンブリッジ、CEO:ミシェル・ヴォナッソス、以下 バイオジェン)は、このたび、抗アミロイドβ(Aβ)プロトフィブリル抗体BAN2401について、患者様856人による臨床第Ⅱ相試験(201試験)の12カ月時点の解析において、ベイジアン解析に基づく成功基準である主要評価項目を満たさなかったと独立データモニタリング委員会が判断したことをお知らせします。
事前に規定したプロトコルに従い本盲検試験を継続し、臨床的に意義ある結果を示すべく、18カ月時点の包括的な最終解析を行います。本最終解析結果は、2018年後半に得られる予定です。
201試験(ClinicalTrials.gov identifier NCT01767311)は、バイオマーカーでAβの脳内蓄積が確認されている、プロドローマルおよび軽度アルツハイマー病(総称して早期アルツハイマー病)患者様を対象とした、プラセボ対照、二重盲検、並行群間比較、無作為化試験です。本試験デザインには安全性と無益性(futility)に関する評価を行う16回の中間解析が含まれており、実施されたすべての中間解析において、これらの中止条件に合致することなく、18カ月の最終解析に向けて試験が継続されています。
今回の12カ月時点のBAN2401の5投与群の有効性の評価は、エーザイが新規に開発した評価指標であるADCOMS(Alzheimer's Disease Composite Score)を用いて行われ、Clinically Significant Difference(BAN2401がプラセボ群と比較して悪化を25%以上抑制)を達成する確率が80%以上になるかどうかが、ベイジアン解析に基づき判定されました。
18カ月時点で行われる最終解析では、ADCOMSに加えて、CDR-SB(Clinical Dementia Rating Sum of Boxes)などの臨床評価指標のベースラインからの変化と共に、アミロイドPETで測定した脳におけるアミロイド蓄積量やvMRIで測定した総海馬体積などのバイオマーカーの変化など、より包括的な評価が行われます。
エーザイ ニューロロジービジネスグループ チーフクリニカルオフィサー兼チーフメディカルオフィサーであるDr. リン・クレイマーは、「ユニークに設計された本試験においてベイジアン統計を用いることで、従来の試験デザインに比較して、より早期に臨床的に意義ある結果を示すことを企図していました。アルツハイマー病の疾患修飾剤の有効性を検討するには、18カ月の治療期間がより適切と考えられており、18カ月時点での最終解析に期待をしています」と述べています。
BAN2401は、バイオアークティックAB(本社:スウェーデン、ストックホルム、CEO:Gunilla Osswald、以下 バイオアークティック)とエーザイの共同研究から得られた、アルツハイマー病に対するヒト化モノクローナル抗体です。2014年3月からエーザイとバイオジェンは共同開発を進めています。
エーザイとバイオジェンは、アルツハイマー病治療剤の共同開発・共同販売に関して、幅広い提携を行っています。
以上
Biogen Safe Harbor Statement
This press release contains forward-looking statements, including statements made pursuant to the safe harbor provisions of the Private Securities Litigation Reform Act of 1995 about results from the Phase 2 study of BAN2401, the potential clinical effects of BAN2401, risks and uncertainties associated with drug development and commercialization, the potential benefits, safety and efficacy of BAN2401, the timing and status of current and future regulatory filings, the anticipated benefits and potential of Biogen's collaboration arrangements with Eisai and the potential of Biogen's commercial business and pipeline programs, including BAN2401, elenbecestat and aducanumab. These forward-looking statements may be accompanied by words such as “aim,” “anticipate,” “believe,” “could,” “estimate,” “expect,” “forecast,” “intend,” “may,” “plan,” “potential,” “possible,” “will” and other words and terms of similar meaning. Drug development and commercialization involve a high degree of risk, and only a small number of research and development programs result in commercialization of a product. Results in early stage clinical trials may not be indicative of full results or results from later stage or larger scale clinical trials and do not ensure regulatory approval. You should not place undue reliance on these statements or scientific data presented.
These statements involve risks and uncertainties that could cause actual results to differ materially from those reflected in such statements, including without limitation, unexpected concerns that may arise from additional data, analysis or results obtained during clinical trials; regulatory authorities may require additional information or further studies, or may fail or refuse to approve or may delay approval of Biogen's drug candidates, including BAN2401, elenbecestat and/or aducanumab; the occurrence of adverse safety events; risks of unexpected costs or delays; uncertainty of success in the development and potential commercialization of BAN2401, elenbecestat and/or aducanumab, which may be impacted by, among other things, failure to protect and enforce Biogen's data, intellectual property and other proprietary rights and uncertainties relating to intellectual property claims and challenges; uncertainty as to whether the anticipated benefits and potential of Biogen's collaboration arrangement with Eisai can be achieved; and third party collaboration risks. The foregoing sets forth many, but not all, of the factors that could cause actual results to differ from Biogen's expectations in any forward-looking statement. Investors should consider this cautionary statement, as well as the risk factors identified in Biogen's most recent annual or quarterly report and in other reports Biogen has filed with the Securities and Exchange Commission. These statements are based on Biogen's current beliefs and expectations and speak only as of the date of this press release. Biogen does not undertake any obligation to publicly update any forward-looking statements, whether as a result of new information, future developments or otherwise.
本件に関する報道関係お問い合わせ先
-
エーザイ株式会社
PR部
-
バイオジェン・インク
パブリック アフェアーズ
<参考資料>
1. BAN2401について
BAN2401は、バイオアークティックとエーザイの共同研究から得られた、アルツハイマー病に対するヒト化モノクローナル抗体です。アルツハイマー病を惹起させる因子の一つと考えられている、神経毒性を有する可溶性のAβ凝集体に選択的に結合して無毒化し、脳内からこれを除去するモノクローナル抗体です。本抗体による治療アプローチは、疾患症状への作用と病態の進行抑制が期待されています。エーザイは、本抗体について、2007年12月にバイオアークティックとのライセンス契約により、全世界におけるアルツハイマー病を対象とした研究・開発・製造・販売に関する権利を獲得しています。また、2014年3月に、エーザイとバイオジェンは、本剤に関する共同開発・共同販促契約を締結し、2017年10月に内容の一部変更契約を締結しています。
2. 201試験(ClinicalTrials.gov identifier NCT01767311)について
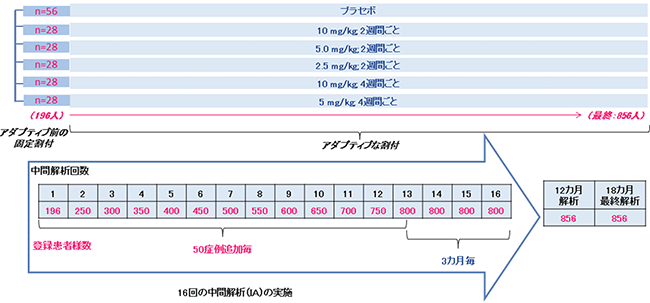
本試験は、BAN2401の有効性及び最適投与レジメンをより効率的に見出すため、中間解析の結果によってより可能性の高い投与群への割付比率をアダプティブに変えるなどの試験途中のデザイン変更を自動的に可能とするベイジアン アダプティブ ランダム化デザインを用い、バイオマーカーによるアミロイド陽性を確認したプロドローマルおよび軽度アルツハイマー病(総称して早期アルツハイマー病)に対するBAN2401の安全性、忍容性、有効性を評価するプラセボ対照、二重盲検、並行群間比較試験です。本試験では、プラセボと実薬5投与群を用い、16回の早期成功を判断する中間解析、12カ月時点でのADCOMSに基づく解析、18カ月時点での包括的な最終解析によって、BAN2401の有効性に関する探索的評価と用量反応性の検討を行います。実薬群5群は、3用量(2.5mg/kg、5mg/kg、10mg/kg)による2週間ごとの投与、2用量(5mg/kg、10mg/kg)による4週間ごとの投与からなります。
投与後12カ月時点の解析では、ADCOMSによるベースラインからの変化を評価するとともに、投与後18カ月時点の最終解析では、ADCOMSに加えてCDR-SBのベースラインからの変化、アミロイドPETで測定した脳におけるアミロイド蓄積量やvMRIで測定した総海馬体積の変化などを包括的に評価します。
3. エーザイとバイオジェンによるアルツハイマー病領域の提携内容について
エーザイとバイオジェンは、アルツハイマー病治療剤の共同開発・共同販売に関して、幅広い提携を行っています。BACE阻害剤elenbecestat*と抗Aβプロトフィブリル抗体BAN2401についてはエーザイ主導のもとで、抗Aβ抗体aducanumabについてはバイオジェン主導のもとで、グローバルでの承認取得に向けた開発を進め、承認取得後は米国、欧州(EU)、日本といった主要市場で共同販促を行います。
両社はelenbecestatとBAN2401に係る研究開発費等の費用を折半し、共同販促に基づく売上高はエーザイに計上され、利益は両社で等しく分配します。
aducanumabについては、2017年10月22日に発効した新たな合意に基づき、2018年3月末までの全ての研究開発費はバイオジェンが負担し、エーザイは、2018年4月から12月末まで15%、2019年1月以降45%の研究開発費用を負担します。販売後、売上に応じて各社が得る地域別利益配分は、バイオジェンは、米国において利益の55%、欧州において68.5%をそれぞれ受領します。エーザイは、日本とアジア(中国、韓国除く)において利益の80%を受領します。その他の地域では利益を折半します。日本とアジア(中国、韓国除く)ではエーザイが売上を計上し、米国、欧州を含むその他の地域ではバイオジェンが売上を計上します。
- *現時点で最終確定したものではありません。
4. エーザイ株式会社について
エーザイ株式会社は、本社を日本に置く研究開発型グローバル製薬企業です。患者様とそのご家族の喜怒哀楽を第一義に考え、そのベネフィット向上に貢献する「ヒューマン・ヘルスケア(hhc)」を企業理念としています。グローバルな研究開発・生産・販売拠点ネットワークを持ち、戦略的重要領域と位置づける「神経領域」「がん」を中心とするアンメット・メディカル・ニーズの高い疾患領域において、世界で約1万人の社員が革新的な新薬の創出と提供に取り組んでいます。
エーザイは、アルツハイマー型認知症・レビー小体型認知症治療剤「アリセプト®」の開発・販売から得た経験を活かし、医療従事者や介護関係者、行政などの協力を得て認知症と共生する「まちづくり」に取り組み、世界で推計1万回以上の疾患啓発イベントを開催してきました。認知症領域のパイオニアとして、次世代治療剤の開発にとどまらず、診断方法の開発やソリューションの提供にも取り組んでいます。エーザイ株式会社の詳細情報は、www.eisai.co.jp![]() をご覧ください。
をご覧ください。
5. バイオジェン・インク(Biogen Inc.)について
神経科学領域のパイオニアであるバイオジェンは、最先端の医学と科学を通じて、重篤な神経学的疾患、神経変性疾患の革新的な治療法の発見および開発を行い、世界中の患者さんに提供しています。1978年にチャールズ・ワイスマン、ノーベル賞受賞者であるウォルター・ギルバートとフィリップ・シャープにより設立されたバイオジェンは、世界で歴史のあるバイオテクノロジー企業であり、多発性硬化症の領域をリードする製品ポートフォリオを持ち、脊髄性筋萎縮症の唯一の治療薬を製品化しました。また、アルツハイマー病、神経免疫疾患、運動性疾患、神経筋障害、痛み、眼科、神経精神医学といった神経領域の研究においても最先端の活動を展開しています。生物製剤の高い技術力を活かし、バイオジェンは高品質のバイオシミラーの製造と製品化にも注力しています。バイオジェン・インクに関する情報については、www.biogen.comおよびSNS媒体Twitter、LinkedIn、Facebook、YouTubeをご覧ください。
6. バイオアークティック(BioArctic AB.)について
バイオアークティックは、スウェーデンに拠点を置き、アルツハイマー病、パーキンソン病のような神経変性疾患の疾患修飾治療や信頼性の高いバイオマーカー・診断薬の開発にフォーカスしたバイオファーマです。また、同社は、完全脊髄損傷に対する治療法の開発も行っています。このようにバイオアークティックは、高いアンメット・メディカル・ニーズがある領域での革新的なな治療の創出にフォーカスしています。大学との共同研究を重視するとともに、アルツハイマー病領域ではエーザイ、パーキンソン病領域ではAbbVieとの戦略的グローバルパートナーシップを形成しています。プロジェクトのポートフォリオは、グローバル企業とのパートナーシップにより資金提供されたプロジェクトとライセンスを企図した社内プロジェクトの組み合わせです。バイオアークティックに関する詳細については、www.bioarctic.comをご覧ください。
